防走失,電梯直達
安全島報人劉亞東A

編輯丨王聰
排版丨水成文
長壽長生是人類永恆的願景。有趣的是,在哺乳動物中,雌性通常比雄性壽命更長,人類也不例外。據世界衛生組織和聯合國人口組織統計,全球範圍內男性平均壽命比女性要短5-10年。據最新統計數據,2022年中國男性平均預期壽命為76.5歲,女性則為82.9歲,差距同樣十分明顯。
2015年,韓國仁荷大學的 Kyung-Jin Min 等人在對公元1392-1910年七劍朝鮮皇家各成員血統紀錄進行仔細分析後發現,一個世紀前,太監(被閹割的男性)也比其他男性活得更久,其平均壽命要比正常男性長14-19年。
不僅如此,閹割延長男性壽命這一觀點在中國的封建王朝歷史中也得到體現。據《中國帝王皇后親王公主世系錄》記載,中國歷代帝王平均壽命只有40歲,而那些服侍他們的太監,平均壽命卻高達71歲。
最近發表的一系列研究成果,揭示了雄性壽命更短背後的「幕後黑手」——雄性激素。
2023年5月23日,德克薩斯大學聖安東尼奧健康科學中心長壽與衰老研究所的 James Nelson教授團隊在Aging Cell期刊發表了題為:Prepubertal castration eliminates sex differences in lifespan and growth trajectories in genetically heterogeneous mice 的研究論文。
該研究證實,青春期前閹割能夠消除了兩性之間的壽命差異,降低了雄性在早年到中年期間的死亡率,延長了雄性的平均壽命,使其與雌性平均壽命相當。

性別在衰老和壽命方面的差異已經被廣泛觀察到,在人類中,女性也通常比男性更長壽。然而,導致這些差異的機制仍然知之甚少。
該研究對UM-HET3小鼠模型進行了研究,該小鼠模型能夠很好地模擬人類壽命的性別差異。研究團隊在這種小鼠模型中探索了青春期後睪丸效應對衰老的性別差異的影響。
結果顯示,在青春期前閹割這種雄性小鼠,能夠消除其兩性之間原本存在的壽命差異,降低了雄性在早年到中年期間的死亡率,延長了雄性的平均壽命,使其與雌性平均壽命相當。
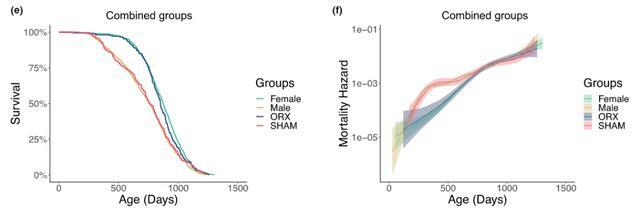
青春期前閹割消除了兩性之間的壽命差異,ORX(閹割),SHAM(假手術)
此外,該研究還發現,閹割後的雄性小鼠儘管生長速率變慢, 但也延長了它們體重增長的持續時間,導致其最終體重遠高於同齡正常雄性。同時也減弱了雄性早期體重和壽命之間的負相關性,使各項指標趨近於雌性。
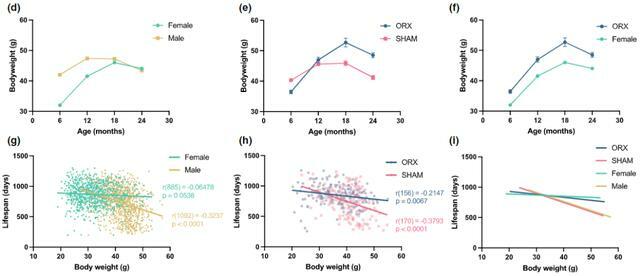
閹割將雄性的生長模式和體重與壽命之間的關係轉變為雌性的水平
這些研究結果表明,青春期後雄性激素是壽命和生長軌跡的性別差異的主要原因。這些發現為進一步研究驅動性別特異性衰老模式的基本機制和開發潛在的長壽干預措施奠定了基礎。
而在2021年7月,eLife 期刊發表的一項研究表明,閹割可以在表觀遺傳層面影響修飾,從而延長壽命。
該研究來自紐西蘭奧塔哥大學和美國加州大學洛杉磯分校等組成的國際研究團隊,論文題為:Castration delays epigenetic aging and feminizes DNA methylation at androgen-regulated loci 。
這項研究顯示,與正常的公羊相比,被閹割的公羊可以延緩DNA衰老,延長壽命。與此同時,這些閹割公羊的DNA甲基化修飾表現出雌性的特徵。研究團隊在綿羊中證實了被閹割的雄性哺乳動物壽命得到延長,並表現其在DNA上表現出相應的特徵。

農民和科學家早就知道,閹割的公羊平均壽命比未閹割的公羊長得多。在這項研究中,研究團隊第一次在DNA層面來研究其背後的原因。
早在2013年,加州大學洛杉磯分校的 Steve Horvath教授聯合了100多個實驗室,對200多種哺乳動物的血液和組織樣本、36000個胞嘧啶甲基化情況進行整理分析,設計出了一個「表觀遺傳時鐘」,這一時鐘可以通過DNA甲基化情況追蹤人類和其他哺乳動物的生物學年齡。
在這項研究中,Steve Horvath教授希望通過「表觀遺傳時鐘」來研究雄性哺乳動物閹割前後的DNA差異,從而揭示閹割延長雄性壽命背後的原因。
研究團隊利用這種「表觀遺傳時鐘」觀察了閹割公羊和正常雄性公羊DNA上的表觀遺傳修飾。他們發現,兩者的「表觀遺傳時鐘」的指針走速是不同的,而且閹割公羊往往要走得更慢。
這意味著被閹割的公羊壽命更長,這一特徵在它們的DNA中得到反映。在綿羊中,雄性和雌性的DNA老化模式非常不同。但令人驚訝的是,閹割的公羊在特定的DNA位點上具有非常雌性化的特徵。
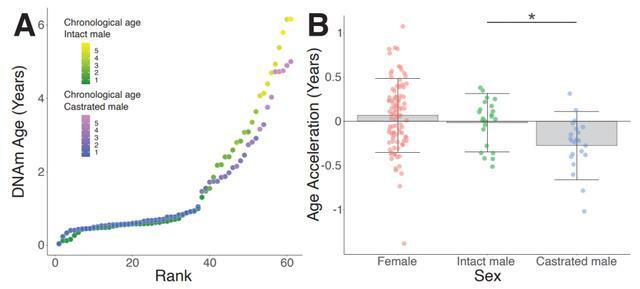
閹割公羊的DNA老化速度更慢
此外,研究團隊還發現,幾種雄性激素敏感的DNA上的CpG島,它們會隨著年齡的增長逐漸呈現出低甲基化趨勢,但在閹割的雄性和正常雌性中保持穩定。類似的性別特異性甲基化差異也存在於蝙蝠皮膚和一系列雄激素受體高表達的小鼠組織中。
這些現象表明,哺乳動物的DNA中存在雄性激素依賴的低甲基化,由此提供了閹割、雄性激素和DNA老化的性別差異之間的明確聯繫。
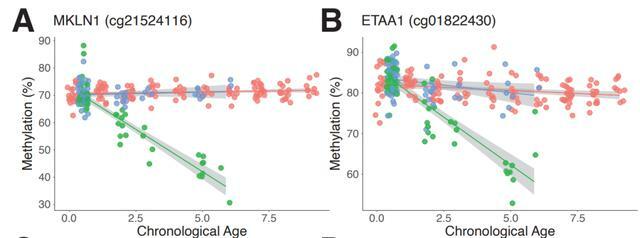
綿羊的DNA中存在年齡相關的、雄性激素依賴的低甲基化
為了了解哪些組織受到雄性激素水平的強烈影響,研究團隊還觀察了小鼠的性別影響。在發現雄性激素受體的組織中,如皮膚、腎臟和大腦,雄性和雌性的DNA模式有很大差異。相比之下,沒有雄性激素受體表達的組織在雄性和雌性中看起來是一樣的。
總的來說,這些研究表明,雄性激素是導致壽命性別差異的關鍵因素,確定這些性別差異背後的機制對於開發相應的延長壽命的靶點至關重要,如果能夠找到既可以消除雄性激素對衰老的有害影響,又不影響雄性功能的靶點,無疑將成為抗衰老和延長壽命領域的大突破。
論文連結:
1. https://onlinelibrary.wiley.com/doi/10.1111/acel.13891
2. https://elifesciences.org/articles/64932
本文經授權轉載自微信公眾號:生物世界(ID: ibioworld),作者生物世界