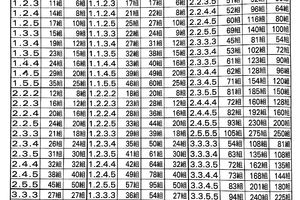
編者按:Hepatitis B Foundation網站B肝新藥表單近幾月未見更新,為幫助大家更準確地獲取全球B肝新藥最前沿信息,肝霖君查詢各大藥企官網更新的產品管線信息和相關網絡資料中的B肝新藥報導做了系統地整理,並匯總了慢B肝新藥與新藥聯合、新藥與現有藥物聯合治療的臨床研究進展。
本期表單更新有:新增處於臨床I期的反義RNA藥物AHB-137。siRNA藥物STSG-0002進入II期臨床;治療性疫苗GS-2829/6779、單克隆抗體KW-027以及HBV RNA去穩定劑AB-161均進入I期臨床。
新藥聯合治療的探索明顯加速,包括新藥與新藥聯合、新藥與現有藥物的聯合。許多新藥單藥在I期或II期研究中未達到主要療效目標,企業便積極開始了不同聯合治療方案的探索。這也將是未來B肝全面臨床治癒的必要策略。

新藥相關聯合用藥臨床研究匯總
部分新藥進展
01 STSG-0002
舒泰神(北京)生物製藥股份有限公司研發的siRNA藥物STSG-0002注射液進入臨床II期(CTR20230448),該項多中心、非隨機化、開放性研究主要為了評價STSG-0002對慢B肝經治患者的安全性和耐受性,次要目的為評價產品的初步有效性;完成該試驗未退出的受試者將開展給藥後5年的長期隨訪研究(CTR20230449)。
02 AHB-137
AHB-137是杭州浩博醫藥有限公司研發的一款注射用反義寡核苷酸(ASO),靶向所有HBV RNA,可引發所有HBV RNA的降解,並在臨床前研究中證明能有效減少HBsAg水平,具有良好的安全性。當前處於I期臨床階段,旨在評估健康志願者和慢B肝患者經單次和多次給藥後的安全性、耐受性、PK特性以及初步療效(NCT05717686),目前已在紐西蘭完成首個隊列給藥。
03 GS-2829/6779(HB-400)
GS-2829/6779是Gilead Sciences使用Hookipa Pharma公司基於沙粒病毒載體的專有TheraT®和Vaxwave®免疫技術研發的兩款治療性B肝疫苗,也即Hookipa Pharma公司的慢B肝項目HB-400。近日Gilead Sciences註冊了一項在健康成人和慢B肝患者中進行的Ia/Ib期臨床試驗(NCT05770895),旨在評估GS-2829/6779治療的安全性和耐受性,目前暫未招募。
04 KW-027
KW-027是北京凱因科技股份有限公司研發的注射用單克隆抗體,據公司宣布,該產品用於慢性B型肝炎治療的I期臨床試驗已獲得國家藥品監督管理局藥品審評中心的默示許可(CXSL2300038)。
05 AB-161
Arbutus Biopharma研發的口服HBV RNA去穩定劑AB-161進入臨床I期(ACTRN12623000074695),這是一項隨機雙盲、安慰劑對照的單劑量研究,旨在評估健康受試者口服AB-161的安全性、耐受性和藥代動力學。
來源:雨露肝霖