(人民日報健康客戶端記者 高瑞瑞)據國家藥監局數據顯示,截至2022年底,在《醫療器械分類目錄》中的1765個二級產品類別下,我國有74項二級類別的產品僅有進口產品註冊證,尚未有國產產品獲批,其中,尚未突破的產品主要集中在有源植入和體外診斷領域,植入式心律轉復除顫器(ICD)仍是註冊證最大的短板,共有46款進口註冊證獲批,無國產註冊證獲批。
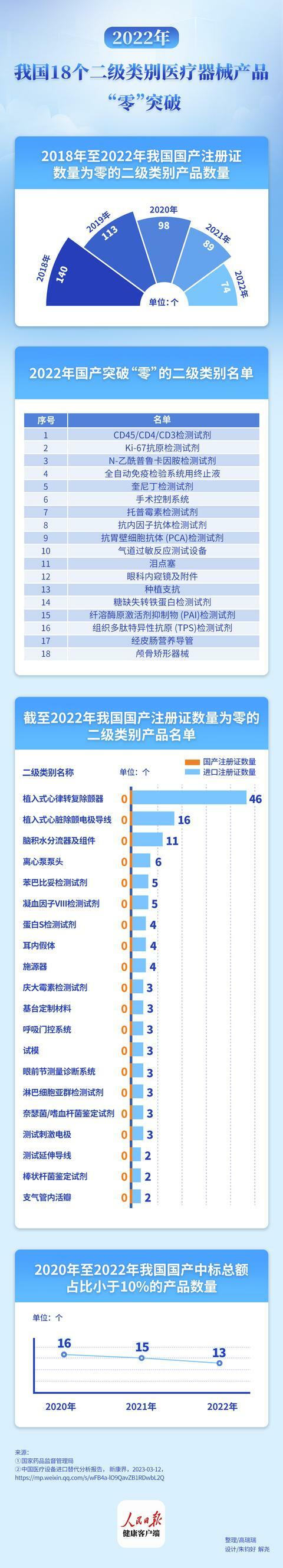
植入型心律轉復除顫器(ICD)是預防心臟性猝死(SCD)最為有效的治療措施。
據國家藥監局網站顯示,目前尚無國產ICD通過上市審批,產品只能依賴進口,國際上ICD主要被美國、德國的公司所壟斷,產品基本只來源於美敦力、雅培(聖猶達)、波士頓科學和百多力四家企業。
「植入型心律轉復除顫器(ICD)屬於專科產品,由於國內的醫療器械起步比較晚,一部分高精尖醫療器械的國產化,需要臨床和生產企業都有意願,以及人才互相配合,才能夠共同的把產品做好。」中國國際旅行衛生保健協會醫療物資與醫療合作分會秘書長陳紅彥告訴人民日報健康客戶端記者,進口替代是國內醫療器械領域不容置疑的發展趨勢,過往許多國產品牌能通過仿製國外產品快速起家,或者通過低端平替產品的策略快速搶占市場。然而ICD的進口替代更難實現,因為相比其他器械,ICD的質量控制更為嚴格,製造工藝更為複雜,被公認為是行業中壁壘最高、系統最複雜、研發最具風險的三類有源植入醫療器械。
根據新思界產業研究中心發布的《2023-2027年中國植入式心律轉復除顫器(ICD)行業市場行情監測及未來發展前景研究報告》顯示,進口ICD價格高昂,不利於市場推廣,在國產替代大趨勢下,ICD國產化將是必然趨勢。目前國內從事ICD研發的企業主要有創領心律醫療、無雙醫療等,其中無雙醫療第二代ICD正處於研發中,其性能指標基本達到國際領先水平。
陳紅彥告訴人民日報健康客戶端記者,我國ICD植入比例較低還與我國特殊國情有很大的關係。一是國內經濟水平雖有較大提升,但居民對心源性猝死風險防範意識薄弱,許多患者對自己的病情並不知曉。二是企業早期主要是生產康復理療類的低值耗材產品,隨著科技的發展才逐步生產一些進口替代產品,相對比較慢。三是ICD價格高昂,全部為進口產品,價格通常達到9萬-14萬,目前醫保報銷比例不高,採用後患者會面臨沉重的經濟負擔。
陳紅彥談到,「當前國產醫療器械研發麵臨著瓶頸,進口產品臨床應用不是很廣,而且很多醫院醫生還沒有普遍使用,所以很多企業國產產品一旦投入研發,巨大的研發成本難以收回,企業有很大的研發壓力。但在這樣的情況下,能夠逐步實現國產替代,已經邁出了一大步,未來確實還需要一段時間。」
陳紅彥建議,隨著我國居民醫療水平的提高,未來國內除顫器市場滲透率提高的同時,也將為這類高端耗材帶來巨大的市場空間,所以類似植入型心律轉復除顫器(ICD)屬於專科產品,僅民營研發力度不夠,國家有關醫療科研院所、臨床醫學專家要有參與科研創新、原研的積極性,從人才、技術、政策等方面做到全方位支持,不僅跟跑、並跑,要把實現領跑作為目標。