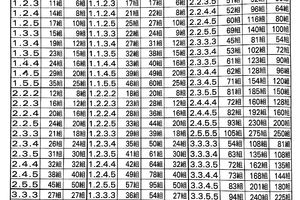
生酮飲食(ketogenic-diet,KD)是一種脂肪高比例、碳水化合物低比例,蛋白質和其他營養素合適的配方飲食。當人們進行生酮飲食時,身體會代謝產生更多的酮體(包括乙醯乙酸、β-羥丁酸和丙酮),以用作能量來源。此時,由於攝入的碳水化合物低,血糖來源少,身體被迫進入「模擬飢餓」的狀態,身體的脂肪會被大量分解,給身體供能,最終讓身體進入一個高速燃脂的狀態,以達到減肥效果。除了用於減肥之外,還有一些研究顯示,生酮飲食可能增加癌症治療效果。
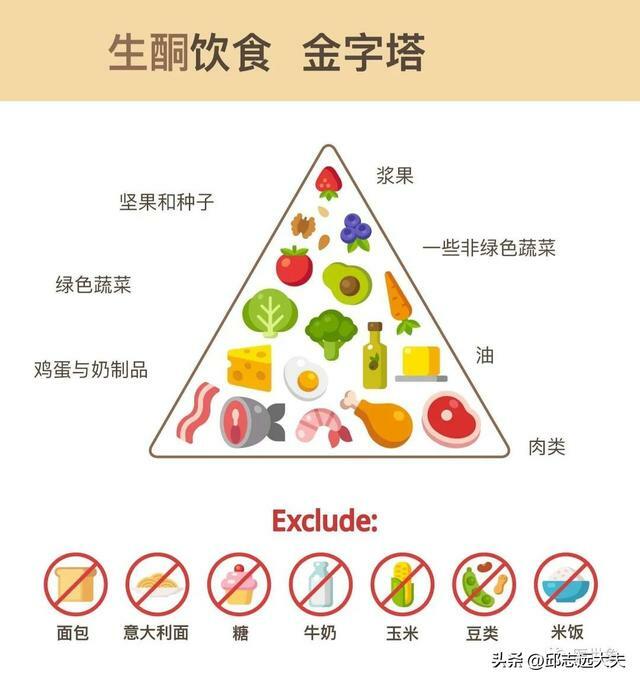
生酮飲食是高脂肪、低碳水化合物、適量蛋白質搭配的飲食方式,其中蛋白質占比20%左右,碳水化合物占比5%-10%,而脂肪占比達到了70%-80%。與正常的膳食結構不同,生酮飲食通過代謝產生酮體供能。
化療相關性血小板減少症(Chemotherapy-induced thrombocytopenia,CIT)是癌症患者接受化療後的常見併發症,這會導致手術複雜化並增加出血風險,還會導致化療劑量減少或停用,從而降低治療效果並導致患者生存受損。臨床數據顯示,每10名接受化療的癌症患者中就有1名出現CIT,這對患者和醫療保健系統來說是一個巨大的負擔。
近日,復旦大學基礎醫學院楊雲龍團隊在 Science 子刊 Science Translational Medicine 上發表了題為:Dietary ketone body–escalated histone acetylation in megakaryocytes alleviates chemotherapy-induced thrombocytopenia 的研究論文,該論文還被選為當期封面論文。
這項研究證明了生酮飲食可以緩解動物和人類的化療相關性血小板減少症(CIT),並且又不會引起血小板增多。

生酮飲食(KD)是一種非常低碳水化合物的飲食模式,已被用於治療癲癇或肥胖。在過去的20年裡,許多研究探索了生酮飲食在各種比病理條件下的治療潛力,包括糖尿病、多囊卵巢綜合徵、先天免疫反應、淋巴水腫和癌症等。現在一致認為生酮飲食對於癌症患者而言是可行和安全的。
從機制上講,生酮飲食導致肝細胞產生酮體,主要是β-羥基丁酸(β-OHB)組成,作為身體的替代能量來源。在肝外組織中,酮體被單羧酸轉運體(MCTs)吸收,然後通過線粒體酶代謝,包括3-β-羥基丁酸脫氫酶(BDH),轉化為乙醯輔酶A,在三羧酸循環中被氧化。
利用生酮來對抗癌症已經成為一個越來越受關注的研究領域,科學家們提出了其抗腫瘤作用的各種可能機制。然而,生酮飲食對腫瘤相關併發症的潛在治療作用還沒有得到足夠重視和研究。
在這項研究中,研究團隊使用各種類型的生酮飲食在多種小鼠模型中研究了生酮飲食對血小板生物發生的影響及其機制。利用化療相關性血小板減少症(CIT)臨床前模型進一步研究了生酮飲食對CIT的預防和治療作用,並對癌症患者的CIT發生率和生酮飲食生活方式進行了回顧性分析。
結果顯示,生酮飲食可以緩解動物和人類的化療相關性血小板減少症(CIT),並且不會引起血小板增多。具體來說,生酮飲食減輕了小鼠模型的CIT,在健康人類志願者中,生酮飲食能夠適度增加血小板數量而又不會引起血小板增多。而在癌症患者中,生酮飲食的生活方式與CIT呈負相關。
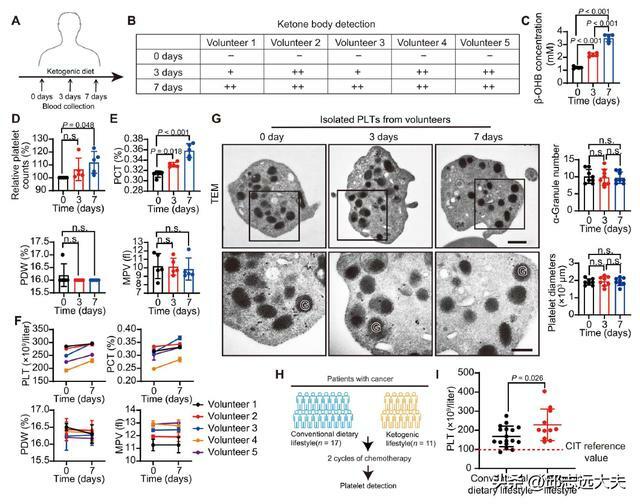
生酮飲食適度增加健康志願者的血小板數量,並與癌症患者的CIT發病率呈負相關
在機制上,生酮飲食誘導循環β-羥基丁酸(β-OHB)增加骨髓巨核細胞組蛋白H3乙醯化。功能獲得和功能喪失實驗顯示,3-β-羥基丁酸脫氫酶(BDH)介導的酮體代謝在促進組蛋白乙醯化中起著獨特的作用,組蛋白乙醯化促進血小板生物發生基因的轉錄並誘導血小板生成。而巨核細胞特異性酮體轉運體單羧酸轉運體1(MCT1)的遺傳缺失或MCT1的藥理靶向阻斷了β-OHB誘導的小鼠血小板生成。
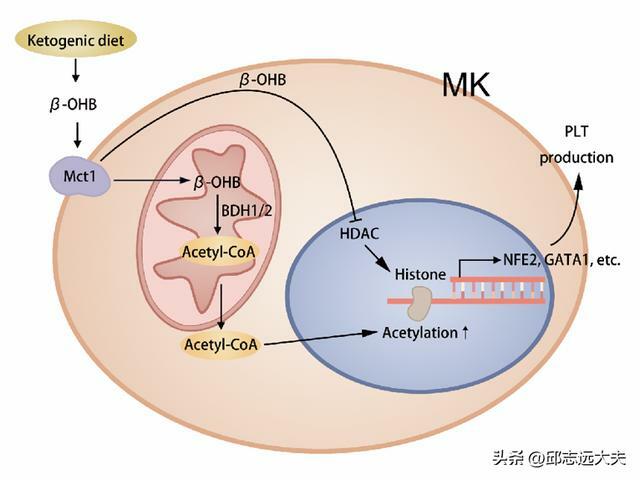
生酮飲食調控血小板生成的機制示意圖
總的來說,該研究提出了在巨核細胞中酮體-MCT1-BDH-組蛋白乙醯化-血小板生成軸的機制見解,並提出了一種無毒、低成本的飲食干預方式來對抗化療相關性血小板減少症(CIT)。
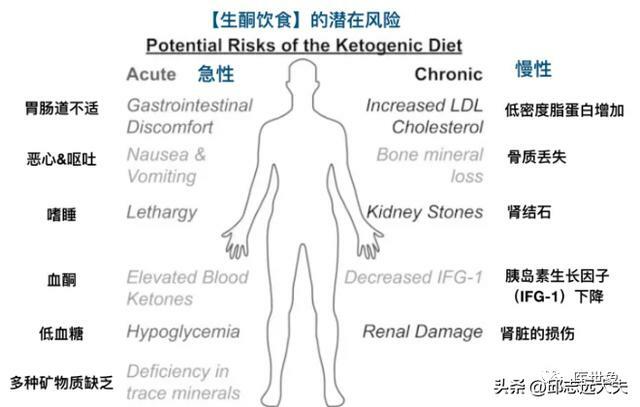
但是也要提醒大家,開始生酮飲食前必須對身體進行全面評估,去專業醫院營養科就診諮詢,調整飲食結構,並跟蹤疾病預後及身體的各項指標情況,務必在專業醫生的指導下進行。
可能與生酮飲食相關的急慢性副作用
復旦大學基礎醫學院楊雲龍研究員為論文通訊作者。復旦大學、福建醫科大學附屬龍巖第一醫院的謝思思博士、復旦大學博士生江晨宇,福建醫科大學附屬龍巖第一醫院的吳勐副教授及同濟大學葉穎副教授為論文共同第一作者。