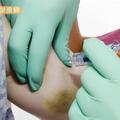
在消費市場上,薑黃及薑黃粉可以說是保健食品產業的寵兒,從線上電商、百貨公司、保健食品專櫃、甚至是一些文青市集,到處都可以看到有人在賣薑黃相關的產品。從整根的薑黃、乾燥的薑黃粉、薑黃膠囊,甚至是混了其他成份的產品像是「薑黃膠原蛋白飲」都有。賣的人把薑黃講到好像可以治百病一樣,從降血糖、降血壓、調節免疫、抗癌、減肥⋯⋯各式各樣的功效都有人宣稱,但到底薑黃有什麼效果,沒有仔細研究其實很難清楚回答出來。因此 MedPartner 團隊的營養師、藥師、醫師們從數千篇相關文獻中挑選,幫大家回顧高達 45 篇文獻,清楚告訴大家有關於薑黃的功效,截至目前為止的研究結果,到底對什麼有效、對什麼沒效,有一分證據說一分話。
如果您是一般民眾,可以閱讀標題跟黑色重點,看你需要的部分就好。如果您是專業醫護人員,需要更進一步的文獻整理,可以看更多有關實驗的說明,讓您在跟民眾衛教相關知識的時候更具實證,也更有信心。希望您收下我們的心意,並將這份整理應用在您的臨床工作中,一起為照顧民眾的健康努力吧:)
因為涉及的可能功效實在太多,您可以選擇全部看完,或者直接滑到您在意的功效部分看過。但請記得一定要看最後的相關結論喔!
薑黃是什麼?什麼食物吃得到薑黃?薑黃怎麼吸收?
薑黃主要生長在南亞、印度、印度尼西亞,它的根部以及地下莖可以磨成粉做為調味料以及天然色素使用。薑黃當中的類薑黃素含量大約占 2-6%,類薑黃素包括了本篇主要討論的薑黃素(Curcumin)以及另外兩種成分 demethoxycurcumin、bisdemethoxycurcumin,它們三者在類薑黃素當中的所佔比例依序為 80%、18% 及 2%。

薑黃素的主要來源就是薑黃,而如同一開始所提到,薑黃粉中的類薑黃素只佔了 2-6%,當中最主要的有效成分薑黃素又只佔了當中的 80% 左右。而在日常生活的食物中,目前僅有咖哩中會使用到薑黃,但其中薑黃的含量並不高。而問題不是只有含量這麼簡單,吃進人體的東西一定要考慮「吸收」,醫學一點的講法叫做「生物可利用率」的問題。
薑黃素的結構式中包括兩個苯酚,因此不易溶於水,較易溶於有機溶劑或油脂。目前想要以口服的方式攝取薑黃來達到健康上的效益仍然有許多挑戰,首先,薑黃的水溶性不佳造成人體吸收率差,再者,它在人體腸道以及肝臟的代謝很快速,所以即便你成功吸收了,在體內也留不太住。薑黃素相關的細胞實驗都可以見到很顯著的結果,但當應用到人體實驗時便不一定能夠得到相同效果,主要就是因為生物可利用率低的緣故。此外,還有研究發現薑黃會因為紫外線照射而受到破壞。

目前有許多研究者,相繼想辦法把薑黃素的生物利用率提高:
(以下這段看起來不太像人話,看不懂可以直接略過,看這三點後面的小結論。)
1.奈米薑黃
研究者將薑黃以奈米膠體的方式製備,將原本顆粒大小約為 22.75um 的薑黃粉縮小至 0.19um,可提高溶解度、且耐光、對熱也很穩定。研究者把 30mg 的奈米薑黃包覆在澱粉製作的膜當中,並搭配 100mL 開水讓受試者攝取,之後抽血檢驗血漿中薑黃的含量,發現奈米薑黃的利用率比薑黃粉增加了 27 倍,大約在攝取後的 30 分鐘血漿中可偵測到的濃度最高,之後便開始下降,到了六小時會稍微提高,爾後就直線下降(Ref 6)。
2.薑黃脂質體
薑黃是脂溶性的成分,因此研究者將薑黃製作成為固體的脂質薑黃顆粒,讓受試者分別攝取含有 650mg 薑黃脂質體的膠囊以及 95% 的薑黃萃取物,攝取薑黃脂質體的受試者在 2 小時後血漿中可偵測到薑黃素的高峰濃度,為 22.43 ng/mL,而薑黃萃取物的組別血漿中則無法偵測到薑黃(Ref 7)。
3.磷脂質複合物
薑黃素因為具有極性基所以可以氫鍵、偶極力和卵磷脂形成複合物。有廠商將薑黃抽出物以 1:2 的比例和卵磷脂結合,在動物實驗中發現此複合物比一般的薑黃吸收率提高了 20 倍以上。人體試驗則讓實驗組受試者分成「攝取低劑量」及「高劑量薑黃–磷脂質複合物」的實驗組,分別攝取約 209mg 以及 376mg 的此複合物;以及攝取 1800mg 一般薑黃素抽出物的控制組。結果發現,控制組血漿中偵測不到薑黃,實驗組則皆偵測得到,其中高劑量組在攝取後的 2 小時,人體血液中濃度可達顛峰,約為 50.3ng/dL,隨後便慢慢下降。整體而言,此產品的人體吸收率比一般的薑黃提高 29 倍。值得注意的是,其中人體血漿中可偵測到含量最高的薑黃抽出物不是薑黃素,而是薑黃當中的另外一個成分 demethoxycurcumin(Ref 8)。
所以這段的重點是:日常食物通常只有咖哩有薑黃,而咖哩料理通常會用到油脂一起烹調,是相對容易吸收的形式。天然薑黃中含有薑黃素,但是薑黃不容易溶於水因此不易吸收,而且還很容易代謝,很難在體內產生高濃度。為了解決這個問題,科學家使用了「奈米化」、「脂質體」、「磷脂質複合物」等方式,來增加人體對薑黃的吸收程度。你如果買整條的薑黃來吃,或者是買一包薑黃粉來泡水喝,基本上你是吸收不了什麼薑黃素的。
有關於薑黃的功效傳說這麼多,以下我們就一項一項分析相關研究結果給你。
薑黃可能有哪些功效?可能沒有哪些功效?
薑黃素(Curcumin)可以說是近年來最多研究者趨之若鶩做研究的物質之一,它是薑黃(Curmuma longa L.)中含有的成分。在這邊我們先說一部分結論:若人體吸收了足夠劑量的薑黃素,確實在某些問題具有一些功效,但網路上你如果看到「薑黃功能打敗西藥」這類的論點,你就先笑笑就算了,實際上目前的研究距離「打敗西藥」還有很大的距離啊~
1.抗發炎
各種分子研究已經證實薑黃素可以抑制促發炎因子,在以脂多醣刺激人類血液的實驗模式中,發現薑黃素可以透過抑制 PGE2 合成酶 1 的活性來減少促發炎細胞激素 PGE2 的生合成(Ref 33);在小鼠巨噬細胞以及人類大腸癌細胞模式中,同樣證實了薑黃素可以抑制由脂多醣所誘發的 COX-2 表現,進而可能減少 PGE2 的生成(Ref 35);在子宮頸癌細胞株的實驗中發現薑黃素會促進癌細胞的凋亡,此外也會抑制 AP-1 以及 NF-kB 的表現(Ref 34);另外一篇小鼠細胞株的實驗則發現薑黃素可以抑制促發炎細胞激素IL-18(Ref 36)。
薑黃素被發現可透過抑制特定酵素的活性,來降低發炎細胞產生的發炎反應。但這些研究結果和實際人體實驗還有距離。
2. 抗氧化
氧化一般來說被認為和人體老化有關,因此抗氧化能力通常被認為是一種抗老化能力。在細胞實驗中發現薑黃素具有透過促進血紅素中的特定酵素表現,產生保護細胞抵抗氧化壓力的功能(Ref 37);在另一個小鼠細胞的實驗中,也發現薑黃素有抗氧化的能力(Ref 38)。在一篇糖尿病小鼠的動物實驗中則發現,攝取薑黃素的小鼠血清中超氧化物歧化酶(SOD)的含量比較多,SOD 是一種抗氧化物。
因此在細胞實驗及動物實驗中,薑黃被認為具有一定的抗氧化能力。
3. 預防心血管疾病
因為發炎是心血管疾病的危險因子之一,薑黃素的抗發炎能力就在心血管疾病的治療上扮演了重要角色。某篇小鼠實驗發現給予有高血壓性心臟疾病的小鼠每公斤體重 50mg 的薑黃素可以預防心臟衰竭。(Ref 23)
這是一篇動物實驗,實際在人體實驗是否能發揮作用的變數仍多。
4. 降低血中膽固醇
ü 一篇研究以 33 位有冠狀動脈疾病的病人為受試者,將其分為控制組以及薑黃素組進行為期 8 週的實驗,控制組每天吃四次安慰劑;薑黃素組則每天吃四次含 500mg 薑黃素的膠囊,本篇使用的薑黃素為Curcumin C3 complex 膠囊。結果發現薑黃素組的三酸甘油酯、低密度膽固醇及極低密度膽固醇介入後都比介入前顯著下降。(Ref 24)
ü 一篇隨機雙盲實驗以 70 位急性冠狀動脈綜合症患者為受試者,分成四組,第一組攝取安慰劑、第二、三、四組每天分別攝取 45mg、90mg、180mg 薑黃素,進行為期 2 個月的介入。結果發現以薑黃素介入之後,不管是在膽固醇、低密度膽固醇、高密度膽固醇以及三酸甘油酯,與介入前都沒有顯著差異。(Ref 25)
ü 一篇較久以前的研究,讓 10 位健康受試者攝取 500mg 的薑黃素膠囊,介入時間為 7 天。結果發現血清脂質過氧化物顯著下降 33%、總膽固醇顯著下降 11.63%、高密度膽固醇則顯著提升 29%。(Ref 26)
綜合以上三篇研究結果而論,薑黃素對於血脂肪的下降效果或許與劑量有關,較低劑量的薑黃素無法有效改善血中的膽固醇或三酸甘油酯,因此想單純靠食物或薑黃粉來改善是不太可能的。
5. 預防糖尿病
研究發現,薑黃素可以減少肝臟的葡萄糖生成,抑制高血糖引起的發炎反應,增加特定基因表現進而增加細胞汲取葡萄糖,因此可以減少胰島素拮抗並降低血糖。早在 1972 年,就有第一篇人體實驗發現薑黃素具有降血糖的潛力。除了糖尿病本身,糖尿病的併發症(包括腎病變以及血管病變)也是目前全球各國面臨的健康問題,占了全世界醫療消耗的很大一部份,而因為糖尿病而死亡的案例主要也都是由併發症導致。
ü 一篇研究以 14 位健康人為受試者進行口服葡萄糖耐受度試驗(OGTT、75g/250mL),在喝糖水前先攝取安慰劑或薑黃素,安慰劑為 560mg 乳糖,實驗組則攝取 170mg 乳糖及 400mg 薑黃素,結果發現喝糖水之後的血糖以及升糖指數在各時間點均沒有顯著差異,而攝取 6g 薑黃素的受試者,在喝糖水後 30 分鐘、 60 分鐘血清中的胰島素,以及 90 分鐘後的胰島素指數(insulinemic index)則是有顯著提升,解釋了薑黃素對於健康人可能有促進胰島素分泌的效果。(Ref 27)
ü 一篇大型的隨機雙盲實驗以 240 位糖尿病前期患者為受試者,分成控制組及實驗組進行為期 9 個月的介入,每天分兩次攝取六顆安慰劑或薑黃素膠囊。本篇研究的使用的薑黃膠囊是以薑黃根部磨粉,乙醇萃取,最終每顆膠囊大約含有 250mg 的類薑黃素,因此實驗組的薑黃素劑量約為 1500mg。結果發現介入後的 3、6、9 個月實驗組的空腹血糖、糖化血色素、口服葡萄糖耐受性試驗的平均值都顯著低於控制組;實驗組血清中的 HOMA-b 到了第 9 個月之後顯著地比控制組高、C-peptide 則顯著比控制組低;臨床上可代表胰島素抗性的 HOMA-IR 在介入後的 3、6、9 個月實驗素組都顯著地比控制組低;脂聯素(adiponectin),一種抗發炎的細胞激素,控制組在介入前後沒有太大變化,實驗組則是在介入後第 3、6 個月都有上升,直到第 9 個月脂聯素的濃度顯著的比控制組高;最終,控制組的受試者在第 6、9、12 個月分別有 11 位、18 位及 19 位進展為糖尿病,實驗組則沒有任何一位受試者進展為糖尿病。(Ref 28)
綜合以上研究,在極高濃度的薑黃素攝取下,可能有控制血糖的效果。但低濃度是否仍有效果未知,另外此研究進行九個月,缺乏長期的追蹤,因此高濃度薑黃素長期攝取的安全性未知。
6. 糖尿病腎病變
ü 一篇隨機雙盲實驗以 40 位有糖尿病腎病變的患者為受試者,分成控制組及實驗組,進行為期 2 個月的介入,其中實驗組每天攝取 3 次 500mg 的薑黃膠囊,每錠中約有 22.1mg 薑黃素;控制組則攝取外觀與實驗組相同的安慰劑。結果發現與介入前相比,實驗組尿液中的 IL-8 以及蛋白質、血清中的 TGF-b 以及 IL-8 都有顯著下降。(Ref 29)
在短期間使用高濃度薑黃素,對於糖尿病腎病變的控制可能有幫助。
7. 糖尿病微血管病變
ü 一篇研究以沒有「動脈粥狀硬化」或「心血管疾病風險因子」的糖尿病患者為受試者,實驗組一天攝取 2 次 Meriva(一種薑黃素與磷脂醯膽鹼複合的產品),每天劑量為 1g,介入時間為 4 週。結果發現介入之後皮膚表面的休息血流量有顯著減少的情況,一般糖尿病微血管病變的患者血流量都會增加,解釋薑黃素對於微血管病變可能有改善的效果;另外也觀察到水腫狀況顯著改善;靜脈—動脈反應(venoarteriolar response)顯著提升;PO2 上升的情形,作者推測可能是由於氧氣擴散到皮膚的狀況較好,且水腫改善的緣故。(Ref 30)
目前的研究顯示薑黃對糖尿病為血管病變可能有幫助,但機制不明確。
8. 肥胖
薑黃素可以抑制絲裂原活化蛋白激酶(MAPK, ERK, JNK, and p38),而這些激酶與 3T3-L1 細胞株分化成為脂肪細胞相關,在已分化的脂肪細胞中也會活化 Wnt/β-catenin 的傳導途徑——而這些都與肥胖密不可分。在白色脂肪組織中,薑黃素可以減少巨噬細胞浸潤、瘦體素;在發炎相關的肥胖,薑黃素可以稱加脂聯素(Adeponectin)的表現,抑制 NF-kB 的活性,因此推測對於肥胖有抑制的效果(Ref 1),但仍需人體試驗來證實。
薑黃對於已知與肥胖相關的酵素抑制或活化有關,理論上可能對於肥胖有抑制效果。但這些研究距離人體試驗還有很大距離,另外肥胖是多重因素影響,想要靠薑黃減重的話現階段還是先別妄想。
9. 克隆氏症(Crohn’s disease)
因免疫受損導致的發炎性腸道疾病主要包括克隆氏症(Crohn’s disease)以及潰瘍性大腸炎(ulcerative colitis),常見的表現方式就是消化系統的慢性發炎。薑黃素可透過許多傳導途徑來調節發炎反應,因此推測對於發炎性腸道疾病就有保護的效果。
ü 一篇前瞻性的開放標籤研究,以 5 位有克隆氏症的患者作為受試者,連續 1 個月每天攝取兩次 550mg 薑黃素,之後 1 個月每天攝取三次,並以 Crohn’s Disease Activity Index 問卷測試做為評估病情的標準,結果發現分數總共下降了 55 分,另外也觀察到 CRP 降低的現象,但因為是樣本數小的開放標籤前瞻性研究,此結果尚待更大型的雙盲實驗來證實(Ref 13)。
10. 潰瘍性大腸炎(ulcerative colitis)
ü 另一篇隨機分配的雙盲實驗,以 89 位潰瘍性大腸炎的病患為受試者,控制組每天早晚各攝取一次安慰劑合併磺胺藥(Sulfasalazine)或 Mesalazine,實驗組則是早晚各攝取 1g 的薑黃素搭配上述兩種藥物,總共持續 6 個月,最後控制組及實驗組的復發率分別為 20.51% 以及 4.65%(Ref 14)。
綜合以上研究,高濃度薑黃素攝取對於抑制發炎性腸道疾病可能有效,但需要更近一步研究證實。
11. 神經退化性疾病:阿茲海默症
已知阿茲海默症患者腦部的氧化傷害以及發炎反應都較為旺盛,而薑黃素抗發炎以及抗氧化的能力已經獲得證實,因此開始出現許多薑黃素以及神經退化性疾病的相關研究。血紅素氧化酶(heme oxygenase, HO-1)是會催化血紅素分解產生膽綠素(biliverdin)、鐵以及一氧化碳的酵素,可透過幫助細胞對抗氧化壓力而達到保護細胞的效果,而研究發現薑黃素可以促進血紅素氧化酶的活性。
ü 一篇隨機雙盲實驗以 34 位阿茲海默症患者為受試者,分成三組,一組攝取 4g 與薑黃同樣顏色的安慰劑、一組攝取 4g 薑黃素、最後一組攝取 1g 薑黃素加 3g 安慰劑,攝取方式讓受試者自行選擇,分為直接以薑黃粉形式和食物混合著吃,或是吞 10 顆膠囊,總共進行為期 6 個月的介入。結果發現 MMSE 在介入前後並沒有差異,同樣的,血清中的 Ab40 也沒有受到薑黃素介入的影響,唯一觀察到有差異的只有血清中的維生素 E 增加,但並不能解釋薑黃素對於阿茲海默症有正面效益。(Ref 21)
ü 一篇隨機實驗以 36 位阿茲海默症患者為受試者,分成控制組、攝取2g 薑黃素以及4g 薑黃素的介入組,總共三組,前 24 週為雙盲實驗,後 24 週則為開放標籤實驗,原本的介入組繼續原本的劑量,控制組則隨機分派攝取 2g 及4g 的薑黃素。本篇使用的薑黃素為 Curcumin C3 Complex® 膠囊,內容成分含有70%~80% 薑黃素、15%~25% demethoxycurcumin、2.5%~6.5% bisdemethoxycurcumin。結果發現介入前後無論是 MMSE、ADAS-Cog score、NPI total score、ADCS-ADL score 都沒有顯著差異,同樣的,各種血清中的生物指標也都沒有差異性。(Ref 22)
由上述研究看起來雖然薑黃素在細胞模式中已經證實可以抑制許多發炎的細胞途徑以及促發炎細胞激素的生成,但當應用到阿茲海默症患者的人體實驗當中,似乎都沒有顯著的效果。這可能跟生物可利用率以及血腦障壁等因素有關。
12. 大腸激躁症
大腸激躁症是一種大腸的慢性疾病,最常見的症狀包括腸絞痛、腹痛、腸脹氣、腹瀉及便秘等等,目前原因尚不明。
ü 一篇單盲、隨機的前瞻性研究以 207 位大腸激躁症患者為受試者,進行為期 8 週的介入,控制組攝取安慰劑,實驗組則又分為低劑量及高劑量組,分別攝取 72mg 以及 144mg 的薑黃,其中有 166 位受試者完成研究。由兩種測試量表評估症狀減緩的情況,一個是 ROME II criteria,另一個為大腸激躁症的生活品質問卷,結果顯示低劑量及高劑量組分數分別降低了 22% 以及 25%,而介入後大腸激躁症的盛行率則分別降低了 53% 以及 60%(Ref 15)。
由上述研究看起來薑黃素對於大腸激躁性的控制有繼續研究發展的潛力。
13. 腸胃道潰瘍
ü 一篇泰國的第二階段臨床試驗以 25 位腸胃道潰瘍患者為受試者,潰瘍部位主要是在胃以及十二指腸,患部大小直徑落在 0.5-1.5cm 之間。薑黃素的劑量為每天 3000mg,分五次攝取,本篇使用的薑黃膠囊是將薑黃的根部曬乾後磨粉以每顆 300mg 的份量用膠囊包覆。4 週後有 12 位患者的潰瘍消失,8 週後有 19 位的潰瘍消失,12 週之後則有 19 位的潰瘍消失,剩下的幾位則表示症狀有緩解的狀況。(Ref 18)
由上述研究看起來短期間高頻率大劑量的薑黃素對腸胃道潰瘍有治療的潛力。
14. 胃幽門桿菌感染
胃幽門桿菌的感染相當常見,且為腸胃道潰瘍常見的原因,最常見的治療方式包括質子幫浦抑制劑以及抗生素,但都會伴隨副作用。
ü 一篇研究以 25 位有位幽門桿菌感染並有消化不良症狀的病患做為受試者,連續 7 天每天攝取兩次 30mg 的薑黃素、100 mg 的bovine lactoferrin、600 mg 的N-acetylcysteine、20 mg 的pantoprazole,結果有只 3 位治癒,其它結果包括介入完的 2 個月之後症狀有顯著減輕的情況;然而血清中的 IgG 以及 G-17 則沒有顯著降低,因此本篇研究的結論認為薑黃素對於消滅胃幽門桿菌是無效的(Ref 19)。
ü 另一篇研究以 36 位有位幽門桿菌感染的患者為受試者,一組攝取以 Omeprazole 為主的三種藥物,療程 1 週;另一組攝取 700mg 的薑黃素,為期 4 週,結果發現藥物組有 78.9% 受試者的胃幽門桿菌被消滅,而薑黃素組只有 1 位受試者成功治療;以胃部切片測試各種促發炎細胞激素包括 IL-8、IL-1b、TNF-a、COX-2,結果薑黃素組沒有任何細胞激素的表現降低(Ref 20)。
上述兩篇研究結果顯示,薑黃素對於胃幽門桿菌的治療似乎目前看起來是無效的。
15. 抗癌症
在細胞實驗以及動物實驗當中,發現薑黃素可以預防癌症的進展主要是透過兩個機制:影響血管新生以及腫瘤生長。而薑黃素抑制腫瘤血管新生則是透過以下多個機制:調節 NF-kB、AP-1、EGR-1 的表現,減弱胰臟癌、頭頸癌細胞株的 IL-8 表現,避免血管內皮生長因子(VEGF)的合成、抑制由 NO 以及 iNOS 調節的血管新生、抑制 COX-2 以及 5-LOX、直接減少血管內皮生長因子以及基礎纖維母細胞生長因子的形成等等。細胞實驗中則發現薑黃素會促進各種動物及人類的癌症細胞株死亡,包括白血病、黑色素瘤、乳癌、大腸癌、卵巢癌、腎臟癌、肺癌以及肝癌細胞(Ref 1)。
ü 一篇以 15 位大腸直腸癌患者為受試者的研究,讓病人在早晨空腹至少 2 小時的情況下攝取含有 0.45~3.6g 薑黃素的膠囊,實驗持續進行至病情惡化或受試者退出實驗,時間最長的受試者維持了 4 個月。此研究結果發現在 3.6g 的組別血液中的 PGE2 在介入第 1 天及第 29 天比初始減少了 62% 以及 57%。在 3.6g 組別的三位受試者在攝取薑黃膠囊後的 1 小時後血液中可偵測到 11.1nmol/L 的薑黃素。由於此研究受試者人數很少,因此結果尚待更大型的研究來再次評估(Ref 10)。
ü 另一篇隨機分組的雙盲實驗則以 126 位診斷為大腸直腸癌患者為受試者,分為控制組及攝取薑黃膠囊的實驗組,實驗組每天攝取 3 次含有 360mg 薑黃的膠囊;控制組則是吃 3 次安慰劑,介入時間直到病人接受手術,因此每位受試者介入時間不同,大約落在 10-30 天之間。結果發現實驗組的病人比起控制組體重有顯著上升的情形,由於體重變化與其他許多因素有關,研究者安排營養師幫忙計算病人攝取的熱量,發現兩組之間沒有顯著差異,而排便狀況則是控制組及實驗組分別各有 8 人及 10 人發生腹瀉情況;此外,實驗組病人血清中的 TNF-a 比起初始值也有顯著下降的情況,控制組則沒有此現象;研究者也使用 TUNEL 染色法以及觀察 DNA 碎片來比較介入前後大腸直腸癌組織當中細胞凋亡的情況,結果顯示實驗組在以薑黃介入後癌組織細胞凋亡的狀況明顯提升,控制組則沒有差異;且在實驗組還觀察到抑制癌細胞增生的 p53 的基因表現上升的情況(Ref 11)。
ü 一篇以 25 位胰臟癌患者為受試者的研究則讓病人每天攝取 8g 的類薑黃素,其中的 7.2g 為薑黃素,介入時間直到病情出現進展為止。與其他多篇研究結果相似,此篇研究發現大部分可在血液中被偵測到的薑黃皆是與葡萄醣醛酸(glucuronide)以及硫酸鹽(sulfate)結合的形式,且量極少,再次顯示了薑黃的低生物利用率;另外發現患者周圍血單核細胞(peripheral blood mononuclear cells)中的 NF-kB、COX-2 以及 pSTAT3 表現有下降的狀況(Ref 12)。
ü 兩篇研究同樣讓胰臟癌受試者攝取 8g 薑黃素合併抗癌藥物 Gemcitabine 使用,第一篇研究的 17 位受試者當中有 5 位因為出現難以忍受的腹痛及腹脹而停止實驗,另外 2 位因為出現腹部症狀而將薑黃素劑量減為 4g,因此第一篇研究的結論認為 8 公克的薑黃素對合併 Gemcitabine 的治療而言劑量可能過高;第二篇研究的 21 位受試者則是都沒有出現毒性反應,以薑黃素介入之後的平均存活時間為 161 天,一年之後的存活率則為 19%,其中 5 位受試者血漿中的薑黃素濃度大約落在 29~412 ng/mL 之間(Ref 9、Ref 32)。
由上述實驗,可推斷高劑量的薑黃素對於癌症的治療可能有發展潛力。
16. 關節炎
關節炎患者的促發炎細胞激素及酵素通常會有調節異常的狀況,其中包括了 TNF-a、IL-1b,以及調節前列腺素(prostaglandins)及白三烯素(leukotrienes)的 COX-2 和脂質氧化酶,因此具有抗發炎能力的薑黃素便被應用在關節炎的治療中。
ü 一篇前瞻性研究以 45 位關節炎患者做為受試者分成三組,分別攝取 500mg 薑黃素、50mg Diclofenac sodium、或兩者合併使用。第一個實驗的主要終點為 Disease Activity Score (DAS) 的分數下降,第二終點則為 American College of Rheumatology (ACR) criteria 下降。三組的 DAS 以及 ACR 皆有顯著下降,有趣的是,單獨攝取薑黃素的組別分數下降的比率最高。本篇使用的薑黃素為 BCM-95,將薑黃素與薑黃中其他非活性成分結合,藉以提高生物利用率(Ref 16)。
ü 另一篇研究以 100 位關節炎患者為受試者,分為控制組及實驗組,實驗組攝取與磷脂醯膽鹼結合的薑黃素 Meriva,早晚各吞一顆 500mg 的錠劑,總共含有 200mg 的薑黃素。8 個月之後 WOMAC score分數下降了 50%,跑步機運動測試結果實驗組比控制組優了將近 3 倍;實驗組受試者血清中的促發炎生物指標包括 IL-1b、IL-6、soluble CD40 ligand、soluble vascular cell adhesion molecule-1 和紅血球沉降率也都有顯著下降的情形。此外,有患者表示攝取 Meriva 之後,吃 NSAID 藥物或其他止痛藥的副作用有減輕的現象(Ref 17)。
由上述研究,高劑量的薑黃的抗發炎能力,對於關節炎可能產生緩解的作用。
17. 憂鬱症
薑黃素之所以會學者認為可能具有抗憂鬱效果,除了因為它本身具有抗發炎、抗氧化能力之外,也因為薑黃素具有其他與憂鬱症病因相關的生物效應,包括:抑制單胺氧化酶活性、會影響血清素及多巴胺的釋放、調節下視丘–腦垂腺–腎上腺軸(hypothalamic–pituitary–adrenal axis)、調節神經營養因子(neurotrophic factors)、海馬迴的神經生成以及神經可塑性(Ref 45)。
ü 一篇 2017 年 6 月才剛發表的整合分析(meta-analysis)篩選了兩千多篇薑黃素與憂鬱症以及自殺相關的論文,排除了非人體試驗的研究、非隨機分組或沒有控制組的研究、與抑鬱(depressive disorder)不相關的研究,最後留下六篇研究做分析,受試者人數總共為 377 位。六篇研究中使用的薑黃素劑量有五篇為每天 1g ,一篇為每天 500mg,兩篇使用的薑黃素為 BCM-95,其中三篇除了將黃素外同時有添加 10 或 50mg 的胡椒鹼,介入時間從 4 週至 6 週不等。統計分析結果顯示,以漢式憂鬱量表評估憂鬱程度,發現攝取薑黃素的實驗組比控制組的憂鬱症狀顯著地改善,且在此六篇研究當中都沒有出現副作用,其中三篇研究同時發現薑黃具有顯著的抗焦慮效果。
但由於目前這六篇研究的介入時間不長,受試者人數也不夠多,因此薑黃的抗憂鬱效果還需要後續更多的研究者來證實(Ref 44)。
薑黃素的安全劑量及毒性
薑黃素被食藥署認為是相對安全的成分,目前沒有毒性反應的報導產生。根據歐洲食物安全管理署的定義,薑黃素的每日足夠攝取量(Adequate daily intake, ADI)為每公斤0-3毫克。
●Lao 等人在 2006 年讓 34 位健康受試者每天攝取 500-12000mg 的薑黃素,使用的是純度達 95% 的 C3 Complex。完成研究的有 24 位受試者,作者並沒有解釋沒完成的 10 位受試者為何離開實驗。結果發現劑量高至 12g,並沒有出現副作用或不良反應。但因為薑黃素會影響部分藥物代謝的酵素,可能會造成 DNA 損傷,並且會與鐵發生螯合反應,因此這部分尚待更多研究來釐清。(Ref 31)
●一篇大腸直腸癌研究中,15 位受試者中有 2 位受試者發生腹瀉的情況,給予的劑量分別為 0.45mg 以及 3.6mg,其中一位給予止瀉藥後繼續實驗,另外一位則離開實驗。血液檢測中則發現其中有 4 位受試者出現鹼性磷酸酶(alkaline phosphatase)上升的狀況;3 位受試者則是乳酸脫氫酶(lactate dehydrogenase)比介入前增加了 150%(Ref 10)。
除了上述兩篇研究之外,大部份研究的受試者對薑黃素的耐受度似乎都算良好,的確也有幾篇研究出現少數幾位受試者有腸胃道的症狀包括腹痛、嘔吐等等,因此薑黃素的安全劑量或許還需要更多的研究來證實。
我該買薑黃來吃嗎?要買哪一種薑黃比較好?
薑黃素的主要來源就是薑黃,而如同一開始所提到,薑黃粉中的類薑黃素只佔了 2-6%,當中最主要的有效成分薑黃素又只佔了當中的 80% 左右,因此光是要靠吃薑黃粉吃到有效劑量是有困難的,吃新鮮的薑黃也是一樣,以上面提到的研究對於降血脂肪的有效劑量 500mg 來說,一天必須吃進 10~31.25g 的薑黃粉,更不用說是其他劑量更高的研究。
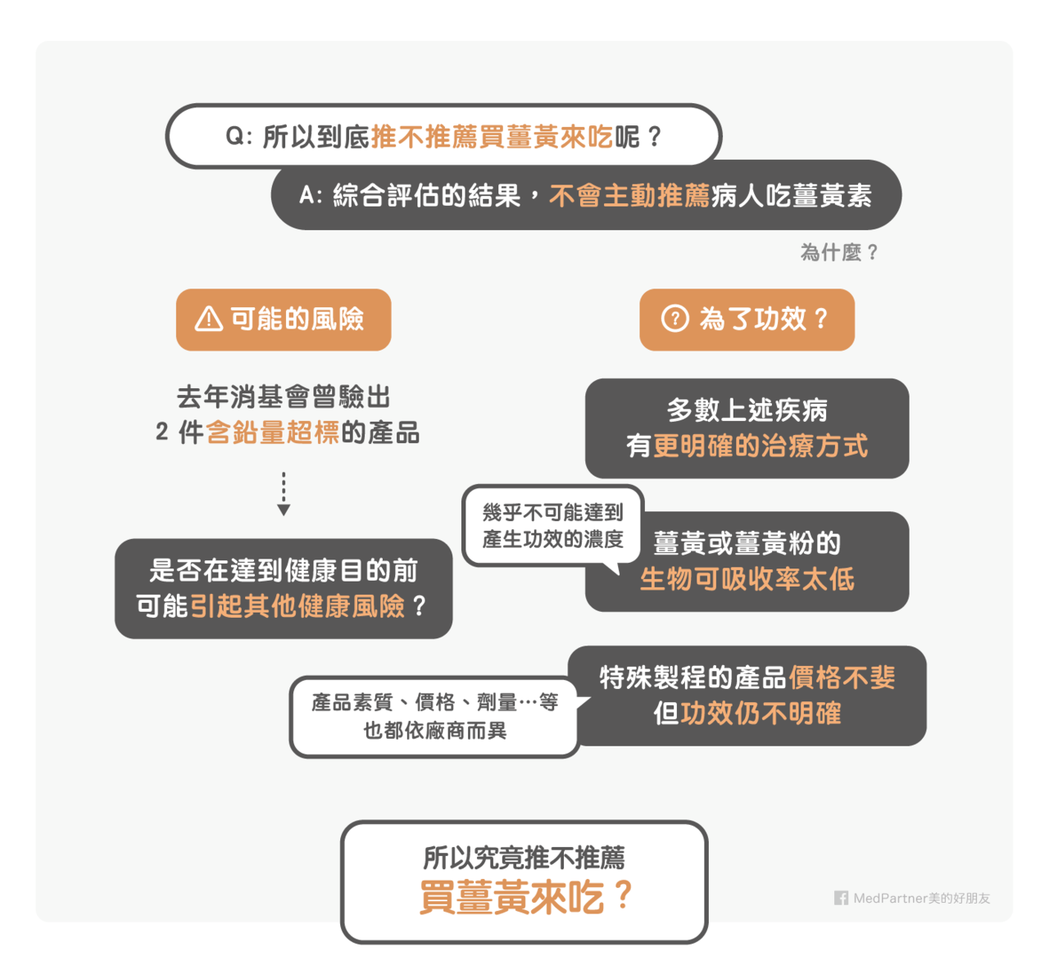
去年底消基會對 19 種市售的薑黃粉做抽查,發現其中有兩件驗出鉛含量超標。因此為了薑黃神奇的功效就趨之若鶩買薑黃粉,開始吃薑黃,是否可能在吃到薑黃的好處之前,就先重金屬中毒了?而若要以產品來說的話,市面上當然已經出現許許多多薑黃素的產品,價格以每罐 1000 元起跳,每種產品每罐的膠囊數量不等,每顆膠囊的薑黃素劑量也不一定。上述多篇研究當中有部分的薑黃都來自於特定的專利商品,雖然研究的成效都很好,但只要有廠商介入,通常結果還是要保持相對高度的質疑。
截至目前為止,我們綜合評讀的結果,並不會因此就主動推薦病人吃薑黃素。主要原因是:
1.多數上述疾病都有更明確的治療方式,不必非要薑黃不可
2.薑黃或薑黃粉可吸收率太低,幾乎不可能達到產生功效的濃度
3.使用特殊製程提高薑黃吸收率的產品,價格通常不斐,但功效仍不明確
4.市售薑黃產品的安全性(是否含重金屬)、可信性(是否含如標示的薑黃素劑量)難以確定
若你真的很想吃,我們只會告訴你,在你經濟許可,身體健康的前提下,我們並不會阻止你,但請注意產品的安全性囉!最後,目前看到的研究中介入時間最長的是 9 個月,若你要持續吃高劑量的薑黃素到超過 9 個月,會有甚麼樣的不良反應還是個未知數囉!雖然目前看起來 9 個月內的安全性是沒啥大問題的,但大家要有一個觀念,「萬物皆有毒」,世界上還沒有一個成分是吃再多再久也不用擔心的,即便是短時間喝下大量的水都可以發生水中毒啊!
如果您覺得評估上述的好處跟風險後,決定要吃薑黃產品,在這邊我們針對以下 8 個族群的朋友們,提出一些注意事項,供您參考。
什麼人可能不適合吃薑黃素?
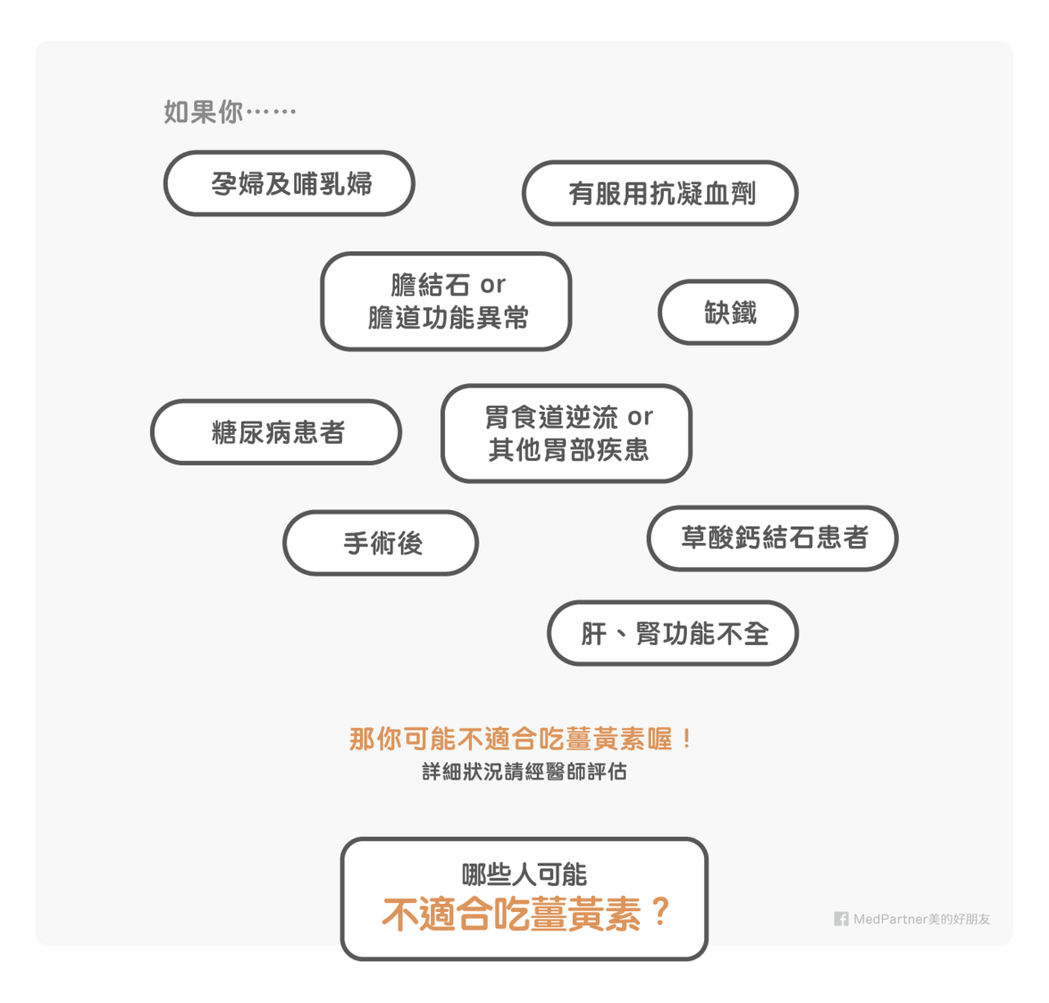
1.孕婦及哺乳婦:目前尚未有薑黃對於懷孕或哺乳婦女安全性的相關研究,若想要攝取建議詢問醫師的意見(Ref 42)。
2.膽結石或膽道功能異常者:薑黃會促進膽汁分泌,因此膽結石或膽道異常患者而言可能不適合補充(Ref42)。
3.有服用抗凝血劑的患者:雖然目前發表的實證醫學文獻中沒有指出薑黃素與抗凝血劑的交互作用,但因為薑黃本身就有抗凝血的功能,所以若您有在服用抗凝血劑,須小心使用薑黃(Ref 43)。
4.糖尿病患者:有服藥的糖尿病患者須小心使用薑黃,因高劑量的薑黃可能具有降血糖的效果,因此若同時有服用降血糖藥物,須小心發生低血糖。
5.胃食道逆流或其他胃部疾病患者:因薑黃會導致部分人出現腸胃道症狀,因此不建議有胃部疾病的人服用薑黃。
6.缺鐵:在細胞模式中發現薑黃會螯合鐵,而在小鼠模式中讓在缺鐵邊緣的小鼠攝取薑黃,發現會讓血比容、血色素、運鐵蛋白飽和度、血清中的鐵全部都下降,且有劑量效應,也發現小鼠肝臟及脾臟中的鐵含量較低,雖然目前尚未有人體實驗證實,不過推測在缺鐵性貧血邊緣或已經有缺鐵性貧血的患者,也許不適合攝取薑黃補充劑(Ref 40)。
7.手術後:因薑黃具有抗凝血活性,因此在手術後不建議攝取。
8.草酸鈣結石患者:人體實驗發現讓健康受試者每天攝取 3.2g 薑黃 4 週後,尿中草酸的濃度會顯度較高,因此建議有草酸鈣結石的患者應避免高劑量的薑黃攝取(Ref 41)。
9.肝、腎功能不全者:安全性仍未知。
花了大量時間完成這份回顧,我們希望廠商們不要紛紛崩潰來罵,我們只是就目前所有可查閱的文獻提出證據判斷。薑黃不是一個「不好」的東西,但不要神化特定的產品,專心致力於更近一步的研究,才能讓這些可能有醫療前景的成分幫助更多人。也希望各位朋友,順手把這篇文章分享給身邊的朋友,讓大家在選購相關產品的時候,有一個安心、可靠,不受業配置入的專業資訊喔!在這邊我們不賣保健食品,但把相關的優缺點分析給大家知道,希望大家能做透過科學證據作出更好的選擇!
Reference:
1.BetÜl Kocaadam & Nevİn Şanlier (2015): Curcumin, an Active Component of Turmeric (Curcuma longa), and Its Effects on Health, Critical Reviews in Food Science and Nutrition, DOI: 10.1080/10408398.2015.1077195.
2.Soheil Zorofchian Moghadamtousi, Habsah Abdul Kadir, Pouya Hassandarvish, Hassan Tajik, Sazaly Abubakar, and Keivan Zandi. (2014) A Review on Antibacterial, Antiviral, and Antifungal Activity of Curcumin. BioMed Research International Volume 2014, Article ID 186864, 12 pages.
3.Preetha Anand, Ajaikumar B. Kunnumakkara, Robert A. Newman, and Bharat B. Aggarwal. (2007) Bioavailability of Curcumin: Problems and Promises. MOLECULAR PHARMACEUTICS VOL. 4, NO. 6, 807–818.
4.Perrone D, Ardito F, Giannatempo G, Dioguardi M, Troiano G, Lo Russo L, DE Lillo A, Laino L, Lo Muzio L. (2015) Biological and therapeutic activities, and anticancer properties of curcumin. Exp Ther Med. 2015 Nov;10(5):1615-1623. Epub 2015 Sep 17.
5.Subash C. Gupta, Sridevi Patchva, and Bharat B. Aggarwal. (2013) Therapeutic Roles of Curcumin: Lessons Learned from Clinical Trials. The AAPS Journal, Vol. 15, No. 1, January 2013.
6.Sasaki H, Sunagawa Y, Takahashi K, Imaizumi A, Fukuda H, Hashimoto T, et al. Innovative preparation of curcumin for improved oral bioavailability. Biol Pharm Bull. 2011;34 (5):660–5.
7.Gota VS, Maru GB, Soni TG, Gandhi TR, Kochar N, Agarwal MG. Safety and pharmacokinetics of a solid lipid curcumin particle formulation in osteosarcoma patients and healthy volunteers. J Agric Food Chem. 2010;58(4):2095–9.
8.Cuomo J, Appendino G, Dern AS, Schneider E, McKinnon TP, Brown MJ, et al. Comparative absorption of a standardized curcuminoid mixture and its lecithin formulation. J Nat Prod. 2011;74(4):664–9.
9.Epelbaum R, Schaffer M, Vizel B, Badmaev V, Bar-Sela G. Curcumin and gemcitabine in patients with advanced pancreatic cancer. Nutr Cancer. 2010;62(8):1137–41.
10.Sharma RA, Euden SA, Platton SL, Cooke DN, Shafayat A, Hewitt HR, et al. Phase I clinical trial of oral curcumin: biomarkers of systemic activity and compliance. Clin Cancer Res. 2004;10(20):6847–54.
11.He ZY, Shi CB, Wen H, Li FL, Wang BL, Wang J. Upregulation of p53 expression in patients with colorectal cancer by administration of curcumin. Cancer Investig. 2011;29 (3):208–13.
12.Dhillon N,Aggarwal BB, Newman RA,Wolff RA, Kunnumakkara AB, Abbruzzese JL, et al. Phase II trial of curcumin in patients with advanced pancreatic cancer. Clin Cancer Res. 2008;14(14):4491–9.
13.Holt PR, Katz S, Kirshoff R. Curcumin therapy in inflammatory bowel disease: a pilot study. Dig Dis Sci. 2005;50(11):2191–3.
14.Hanai H, Iida T, Takeuchi K, Watanabe F, Maruyama Y, Andoh A, et al. Curcumin maintenance therapy for ulcerative colitis: randomized, multicenter, double-blind, placebo-controlled trial. Clin Gastroenterol Hepatol. 2006;4(12):1502–6.
15.Bundy R, Walker AF, Middleton RW, Booth J. Turmeric extract may improve irritable bowel syndrome symptomology in otherwise healthy adults: a pilot study. J Altern Complement Med. 2004;10(6):1015–8.
16.Chandran B, Goel A. A randomized, pilot study to assess the efficacy and safety of curcumin in patients with active rheumatoid arthritis. Phytother Res. 2012;26(11):1719–25.
17.Belcaro G, Cesarone MR, Dugall M, Pellegrini L, Ledda A, Grossi MG, et al. Efficacy and safety of Meriva(R), a curcuminphosphatidylcholine complex, during extended administration in osteoarthritis patients. Altern Med Rev. 2010;15(4):337–44.
18.Prucksunand C, Indrasukhsri B, Leethochawalit M, Hungspreugs K. Phase II clinical trial on effect of the long turmeric (Curcuma longa Linn) on healing of peptic ulcer. Southeast Asian J Trop Med Public Health. 2001;32(1):208–15.
19.Di Mario F, Cavallaro LG, Nouvenne A, Stefani N, Cavestro GM, Iori V, et al. A curcumin-based 1-week triple therapy for eradication of Helicobacter pylori infection: something to learn from failure? Helicobacter. 2007;12(3):238–43.
20.Koosirirat C, Linpisarn S, Changsom D, Chawansuntati K, Wipasa J. Investigation of the anti-inflammatory effect of Curcuma longa in Helicobacter pylori-infected patients. Int Immunopharmacol. 2010;10(7):815–8.
21.Baum L, Lam CW, Cheung SK, Kwok T, Lui V, Tsoh J, et al.Six-month randomized, placebo-controlled, double-blind, pilot clinical trial of curcumin in patients with Alzheimer disease. J Clin Psychopharmacol. 2008;28(1):110–3.
22.J. M. Ringman, S. A. Frautschy, E. Teng et al., “Oral curcumin for Alzheimer’s disease: tolerability and efficacy in a 24-week randomized, double blind, placebo-controlled study,” Alzheimer’s Research &Therapy, vol. 4, p. 43, 2012.
23.Morimoto T., Sunagawa Y., Kawamura T., Takaya T., Wada H., Nagasawa A., et al. (2008). The dietary compound curcumin inhibits p300 histone acetyltransferase activity and prevents heart failure in rats. J. Clin. Invest. 118, 868–878.
24.Mirzabeigia P., Mohammadpour AH, Salarifar M., Gholami K., Mojtahedzadeh M., Javadi MR (2015). The Effect of Curcumin on some of Traditional and Non-traditional Cardiovascular Risk Factors: A Pilot Randomized, Double-blind, Placebo-controlled Trial. Iranian Journal of Pharmaceutical Research 14 (2): 479-486.
25.Alwi I, Santoso T, Suyono S, Sutrisna B, Suyatna FD, Kresno SB, et al. The effect of curcumin on lipid level in patients with acute coronary syndrome. Acta Med Indones. 2008;40(4):201–10.
26.Soni KB, Kuttan R. Effect of oral curcumin administration on serum peroxides and cholesterol levels in human volunteers. Indian J Physiol Pharmacol. 1992;36(4):273–5.
27.Wickenberg J, Ingemansson SL, Hlebowicz J. Effects of Curcuma longa (turmeric) on postprandial plasma glucose and insulin in healthy subjects. Nutr J. 2010;9:43.
28.Chuengsamarn S, Rattanamongkolgul S, Luechapudiporn R, Phisalaphong C, Jirawatnotai S. Curcumin extract for prevention of type 2 diabetes. Diabetes Care. 2012;35(11):2121–7.
29.Khajehdehi P, Pakfetrat M, Javidnia K, Azad F, Malekmakan L, Nasab MH, et al. Oral supplementation of turmeric attenuates proteinuria, transforming growth factor-beta and interleukin-8 levels in patients with overt type 2 diabetic nephropathy: a randomized, double-blind and placebo-controlled study. Scand J Urol Nephrol. 2011;45(5):365–70.
30.Appendino G, Belcaro G, Cornelli U, Luzzi R, Togni S, Dugall M, et al. Potential role of curcumin phytosome (Meriva) in controlling the evolution of diabetic microangiopathy. A pilot study. Panminerva Med. 2011;53(3 Suppl 1):43–9.
31.Lao CD, Ruffin MT, Normolle D, Heath DD, Murray SI, Bailey JM, et al. Dose escalation of a curcuminoid formulation. BMC Complement Altern Med. 2006;6:10.
32.Kanai M, Yoshimura K, Asada M, Imaizumi A, Suzuki C, Matsumoto S, et al. A phase I/II study of gemcitabine-based chemotherapy plus curcumin for patients with gemcitabineresistant pancreatic cancer. Cancer Chemother Pharmacol. 2011;68(1):157–64.
33.Koeberle A, Northoff H and Werz O: Curcumin blocks prostaglandin E2 biosynthesis through direct inhibition of the microsomal prostaglandin E2 synthase‑1. Mol Cancer Ther 8: 2348‑2355, 2009.
34.Divya CS and Pillai MR: Antitumor action of curcumin in human papillomavirus associated cells involves downregulation of viral oncogenes, prevention of NF‑kB and AP‑1 translocation and modulation of apoptosis. Mol Carcinog 45: 320‑332, 2006.
35.Hong J, Bose M, Ju J, Ryu JH, Chen X, Sang S, Lee MJ and Yang CS: Modulation of arachidonic acid metabolism by curcumin and related beta‑diketone derivatives: Effects on cytosolic phospholipase A (2), cyclooxygenases and 5‑lipoxygenase. Carcinogenesis 25: 1671‑1679, 2004.
36.Yadav R, Jee B and Awasthi SK: Curcumin suppresses the production of pro‑inflammatory cytokine interleukin‑18 in lipopolysaccharide stimulated murine macrophage‑like cells. Indian J Clin Biochem 30: 109‑112, 2015.
37.Motterlini R, Foresti R, Bassi R and Green CJ: Curcumin, an antioxidant and anti‑inflammatory agent, induces heme oxygenase‑1 and protects endothelial cells against oxidative stress. Free Radic Biol Med 28: 1303‑1312, 2000.
38.Scapagnini G, Colombrita C, Amadio M, D’Agata V, Arcelli E, Sapienza M, Quattrone A and Calabrese V: Curcumin activates defensive genes and protects neurons against oxidative stress. Antioxid Redox Signal 8: 395‑403, 2006.
39.Miao M, Guo L, Tian S and Wang T: Effects of curcumin on antioxidation in diabetic rats. Pak J Pharm Sci 28 (Suppl 1): 371‑373, 2015.
40.Yan Jiao, John Wilkinson IV, Xiumin Di, Wei Wang, Heather Hatcher, Nancy D. Kock, Ralph D’Agostino Jr, Mary Ann Knovich, Frank M. Torti and Suzy V. Torti. Curcumin, a cancer chemoprevent and chemotherapeutic agent, is a biologically active iron chelator. Blood, 8 Januay 2009 Volume 113, Number 2: 462-469.
41.Tang M, Larson-Meyer DE, Liebman M. Effect of cinnamon and turmeric on urinary oxalate excretion, plasma lipids, and plasma glucose in healthy subjects. Am J Clin Nutr. 2008 May;87(5):1262-7.
42.Gary N. Asher, MD, MPH; Kevin Spelman, PhD. Clinical Utility of Curcumin Extract. Alternative therapies, mar/apr 2013, Vol. 19, NO.2: 20-22.
43.AM Heck, BA DeWitt and AL Lukes. Potential interactions between alternative therapies and warfarin. American Journal of Health-System Pharmacy July 2000, 57 (13) 1221-1227.
44.Qin Xiang Ng, Shawn Shao Hong Koh, Hwei Wuen Chan MBBS, MMed, Collin Yih Xian Ho MBBS. Clinical Use of Curcumin in Depression: A Meta-Analysis. JAMDA 18 (2017) 503-508.
45.Fernanda Neutzling Kaufmann, Marta Gazal, Clarissa Ribeiro Bastos, Manuella PintoKaster, Gabriele Ghisleni. Curcumin in depressive disorders: An overview of potential mechanisms, preclinical and clinical findings. European JournalofPharmacology784(2016)192–198.